2. 楚雄医药高等专科学校 医学检验系, 云南 楚雄 675005;
3. 华东师范大学 上海市城市化生态过程与生态恢复重点实验室, 上海 200241
2. Department of Medical Laboratory, Chuxiong Medical College, Chuxiong Yunnan 675005, China;
3. Shanghai Key Laboratory for Urban Ecological Processes and Eco-Restoration, East China Normal University, Shanghai 200241, China
上海城市内河多属于感潮型河道, 目前由于受人为活动严重干扰, 许多河道出现了季节性或常年性的黑臭问题, 其中底泥内源污染已成为河道水质恶化和发生黑臭的主要原因, 而且感潮特征往往加重内源污染的影响作用[1].这主要是因为涨落潮的水流扰动会使表层底泥反复扬起, 导致底泥中铁、硫和氮污染物的悬浮释放; 另外泥水界面好氧-缺氧-厌氧分布在潮汐作用下也不断变化, 进而影响底泥中铁、硫和氮污染物的迁移转化过程[1-3].
硫和铁是河道致黑致臭的主要元素[4], 氮元素是重要的营养盐元素, 硫、铁与氮元素在调节水生环境质量及生物生产力方面有重要的联系.因此研究感潮型重污染河道底泥中硫、铁元素的环境行为与氮行为的耦合作用对于感潮型河道底泥内源污染物的有效控释具有重要意义[5-6].然而目前相关研究主要针对海洋、河口海岸以及湖泊沉积物, 且忽视了硫、铁与氮之间的耦合关系, 对于污染严重的感潮型城市内河河道的相关研究尚未见诸报道.
本研究针对上海市的重污染感潮型河道, 通过感潮模拟实验探究感潮过程中不同形态氮、硫和铁的动态变化以及内源硫、铁与氮行为的耦合作用, 以期为重污染感潮型河道的治理和修复提供参考.
1 材料与方法 1.1 研究对象本研究上覆水和底泥均采自与上海市普陀区桃浦镇境内的工业河.该河总长864 m, 上口宽度为10~15 m, 水深1~2 m, 水流速度缓慢导致水动力条件较差, 且底泥内源污染严重, 是一条典型的感潮型重污染河道.工业河具体地理位置及采样地点如图 1所示.

|
图 1 采样点地理位置图 Fig.1 Location of the Taopu River and the sampling sites |
工业河上覆水基本理化指标如表 1所示, 其水质基本上低于地表水Ⅴ类水标准.
| 表 1 采样点上覆水基本理化性质 Tab.1 Physiochemical characteristics of the overlying water at the sampling sites |
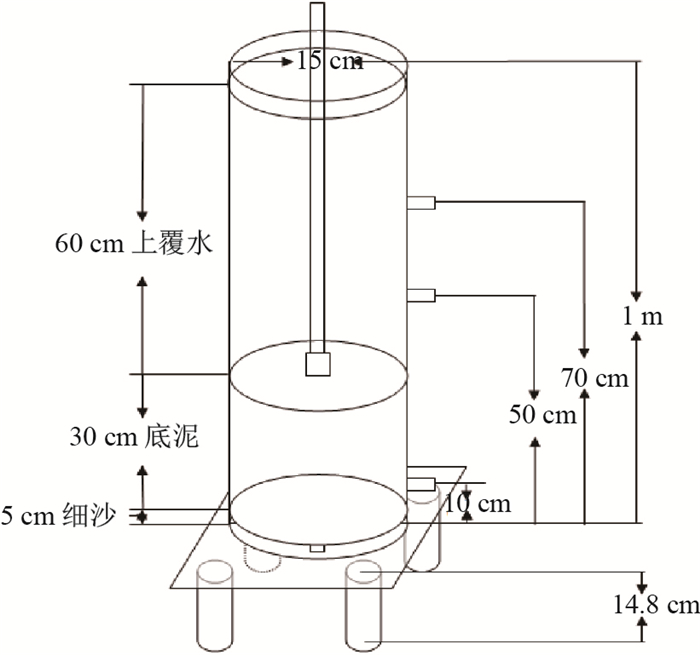
本实验采用感潮河道模拟柱如图 2所示, 底部铺设5 cm细沙, 底泥厚度为30 cm, 并设置对照组(静置组).本实验中感潮河道涨落潮模拟流速及涨落潮最低最高水位是根据前期现场调研情况进行确定, 且因其流速度缓慢、水动力条件较差, 涨落潮模拟装置设置流速较低, 涨潮平均流速约为0.003 cm/s, 退潮平均流速约为0.001 cm/s, 每天模拟两次退潮和两次涨潮, 其中退潮平均历时8 h, 涨潮历时4 h.通过蠕动泵将模拟河道中水样抽入或抽出实验柱实现水位涨落变化.泵的开启采用PLC自动控制, 并通过调节泵流量大小控制涨落潮流速.实验柱上覆水的最低高度为40 cm, 以此模拟退潮时最低水位; 最高高度为60 cm, 以此来模拟涨潮时的最高水位.
|
图 2 感潮型河道模拟装置图 Fig.2 Sketch of experimental setup for the tidal river simulation system |
本试验所涉及的常规理化指标除氧化还原电位(ORP)值、溶解氧(DO)浓度、温度(
本研究中氮与硫铁的耦合关系借助Data Processing System (DPS)数据处理系统采用灰色关联度分析法(General grey reational analysis, GRA)进行解析. GRA是一种因素分析方法, 是在不完全的信息中, 对所要分析研究的各因素进行比较分析, 找出它们的关联程度, 发现主要矛盾, 找到主要特性和主要影响因素. GRA对一个系统发展变化态势进行量化, 非常适合动态的历程分析, 主要分为以下6步骤[8-9]:
①确定反映系统行为特征的参考数列和影响系统行为的比较数列;
②对参考数列和比较数列进行无量纲化处理; ③始点零化件的计算;
④灰色绝对关联度(
本研究利用GRA解析感潮模拟组S
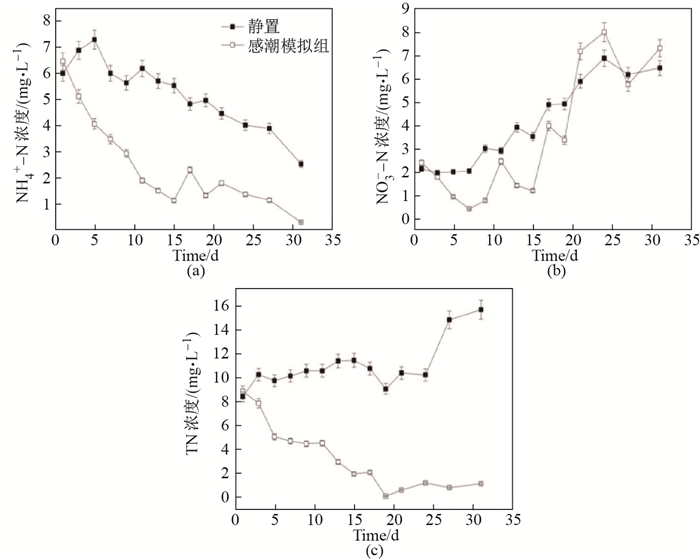
感潮型重污染河道上覆水中不同形态氮的变化如图 3所示.静置组和感潮模拟组NH
|
图 3 感潮型河道上覆水中NH |
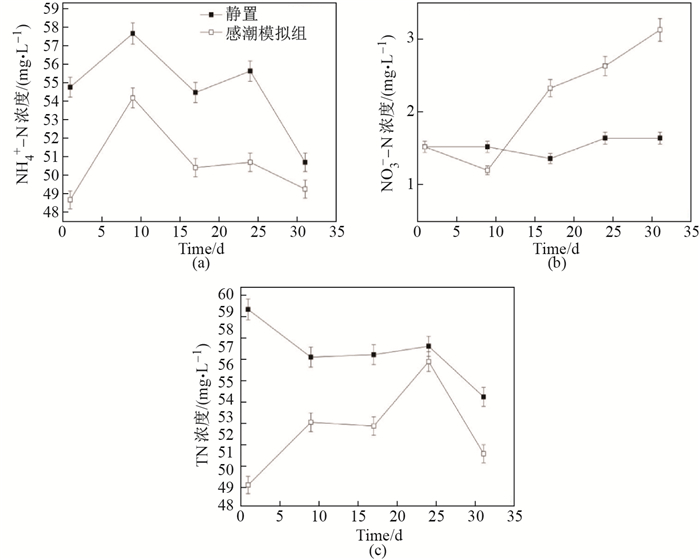
感潮型重污染河道间隙水中不同形态氮的变化如图 4所示.静置组的运行稳定期相较运行初始时的NH
|
图 4 感潮型河道间隙水中NH |
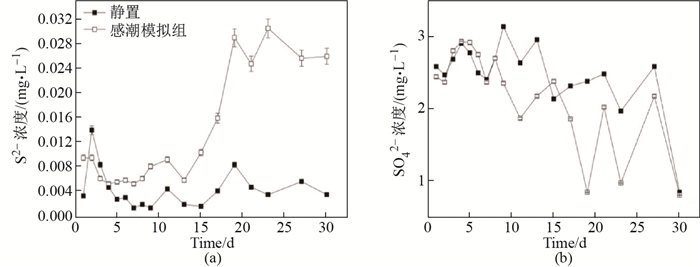
感潮型河道上覆水中不同形态硫的变化如图 5所示.感潮模拟组上覆水S
|
图 5 感潮型河道上覆水中S2-(a)和SO42-(b)的变化 Fig.5 Variations of S2-(a) and SO42-(b) in overlying water for the simulated tidal system |
感潮型河道间隙水中不同形态硫的变化如图 6所示. 感潮模拟组与静置组间隙水硫化物均呈上升趋势(见图 6(a)), 静置组S2-浓度由运行初始的0.10 mg·L-1增加至(0.085±0.003) mg·L-1, 感潮模拟组S2-浓度由运行初始的0.015 mg·L-1增加至(0.090±0.002) mg·L-1, 两组S2-浓度差别较小. 静置组和感潮模拟组SO42-水平波动幅度较大(见图 6(b)), 静置组运行稳定期SO42-浓度较运行初始期有所上升, 由(3.37±0.07) mg·L-1上升至(15.24±0.30) mg·L-1. 感潮模拟组运行稳定期SO42-浓度较运行初始期有所下降, 由(11.18±0.11) mg·L-1下降至(7.09±0.07) mg·L-1.

|
图 6 感潮型河道间隙水中S2-(a)和SO42-(b)的变化 Fig.6 Variations of S2-(a) and SO42-(b) in interstitial water for the simulated tidal system |
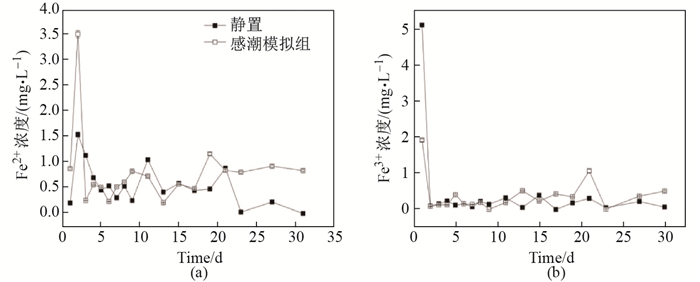
感潮型河道上覆水中不同形态铁的变化如图 7所示. 静置组上覆水中的Fe2+含量总体呈下降趋势, 而感潮模拟组上覆水Fe2+在运行后期浓度有所增长(见图 7(a)). 上覆水Fe3+浓度的变化都大致呈先下降后趋于稳定的趋势, 并且感潮模拟组上覆水的Fe3+水平高于静置组(见图 7(b)). 潮汐作用引起的水体扰动使得底泥中一些与Fe2+结合的物质(如FeS, FeS2等)再悬浮释放, 且潮汐作用有利于Fe3+还原成Fe2+[14-15], 从而使得上覆水中Fe2+浓度有所增长.
|
图 7 感潮型河道上覆水中Fe |
感潮型河道间隙水中不同形态铁的变化如图 8所示.静置组和感潮模拟组运行稳定期较运行初始期间隙水中的Fe

|
图 8 感潮型河道间隙水中Fe |
利用GRA解析内源氮与硫铁环境行为的耦合关系可得到不同形态硫(S
|
表 2 上覆水及间隙水各内源氮与硫铁(S |
对于系统中上覆水NH
通过灰色关联分析可知, 上覆水NO
异于传统反硝化, 硫(铁)自养反硝化过程以还原态硫(铁)为电子供体, 硝态氮为电子受体.感潮模拟实验中, 一方面, 潮汐作用促进了硫酸盐还原为硫化物及三价铁还原为二价铁的过程, 为硫(铁)自养反硝化提供可能的电子供体.另一方面, 水流扰动使得底泥中还原态化合物(如FeS, FeS
上覆水及间隙水NH
感潮型重污染河道长期的潮汐作用会引起的水体反复扰动并促进底泥污染物(如FeS和FeS
硫自养反硝化与铁自养反硝化作可以在脱除内源氮的同时, 将河道底泥致黑致臭物质(FeS
| [1] |
余光伟, 雷恒毅, 刘广立, 等. 重污染感潮河道底泥释放特征及其控制技术研究[J]. 环境科学报, 2007, 27(9): 1476-1484. |
| [2] |
余光伟.重污染感潮河道底泥原位修复技术与工程应用研究[D].广州: 中山大学, 2007. http://www.wanfangdata.com.cn/details/detail.do?_type=degree&id=Y1406710
|
| [3] |
雷恒毅, 余光伟, 刘广立, 等. 珠江流域重污染感潮河道黑臭治理新技术[J]. 中山大学学报(自然科学版), 2007, 46(3): 134-136. DOI:10.3321/j.issn:0529-6579.2007.03.033 |
| [4] |
李真, 黄民生, 何岩, 等. 铁和硫的形态转化与水体黑臭的关系[J]. 环境科学与技术, 2010, 33(6): 1-3. |
| [5] |
李文超, 王文浩, 何岩, 等. 黑臭河道沉积物中硫铁行为与氮磷循环的耦合机制[J]. 华东师范大学学报(自然科学版), 2015, 2(1): 1-8. DOI:10.3969/j.issn.1000-5641.2015.01.001 |
| [6] |
李文超.曝气扰动下城市黑臭河道底泥内源硫、铁行为与氮循环耦合作用研究[D].上海: 华东师范大学, 2016. http://cdmd.cnki.com.cn/Article/CDMD-10269-1016138375.htm
|
| [7] |
国家环保局《水和废水监测分析方法》编委会. 水和废水监测分析方法[M]. 4版. 北京: 中国环境科学出版社, 2002.
|
| [8] |
陈玉霞.曝气复氧条件下黑臭河道底泥内源氮的迁移转化行为研究[D].上海: 华东师范大学, 2007. http://cdmd.cnki.com.cn/article/cdmd-10269-1011131376.htm
|
| [9] |
HE Y, CHEN Y X, ZHANG Y F, et al. Role of aerated turbulence in the fate of endogenous nitrogen from malodorous river sediments[J]. Environmental Engineering Science, 2013, 30(1): 11-16. DOI:10.1089/ees.2011.0538 |
| [10] |
何岩, 沈叔云, 黄民生, 等. 城市黑臭河道底泥内源氮硝化-反硝化作用研究[J]. 生态环境学报, 2012, 21(6): 1166-1170. |
| [11] |
李志洪.曝气扰动模式对黑臭河道底泥内源营养盐行为的影响作用及氮转化功能菌群响应规律研究[D].上海: 华东师范大学, 2015. http://cdmd.cnki.com.cn/Article/CDMD-10269-1015339420.htm
|
| [12] |
尹洪斌.太湖沉积物形态硫赋存及其与重金属和营养盐关系研究[D].南京: 中国科学院南京地理与湖泊研究所, 2008. http://www.wanfangdata.com.cn/details/detail.do?_type=degree&id=Y1615636
|
| [13] |
焦涛.城市河道沉积物-水体系硫化物赋存特征及反硫化过程研究[D], 南京: 河海大学, 2007. http://cdmd.cnki.com.cn/Article/CDMD-10294-2007167921.htm
|
| [14] |
李伟杰, 汪永辉. 铁离子在水体中价态的转化及其与河道黑臭的关系[J]. 净水技术, 2007, 26(2): 35-37. DOI:10.3969/j.issn.1009-0177.2007.02.011 |
| [15] |
尹洪斌, 范成新, 李宝, 等. 太湖北部沉积物中铁硫的地球化学特征研究[J]. 地球化学, 2008, 37(6): 595-601. DOI:10.3321/j.issn:0379-1726.2008.06.010 |
| [16] |
TORRENTÓ C, URMENETA J, OTERO N, et al. Enhanced denitrification in groundwater and sediments from a nitrate-contaminated aquifer after addition of pyrite[J]. Chemical Geology, 2011, 287(1/2): 90-101. |
| [17] |
JUNCHER JØRGENSEN C, JACOBSEN O S, ELBERLING B, et al. Microbial oxidation of pyrite coupled to nitrate reduction in anoxic groundwater sediment[J]. Environmental Science & Technology, 2009, 43(13): 4851-4857. |
| [18] |
YANG X N, HUANG S, WU Q H, et al. Nitrate reduction coupled with microbial oxidation of sulfide in river sediment[J]. Journal of Soils Sediments, 2012, 12(9): 1435-1444. DOI:10.1007/s11368-012-0542-9 |
| [19] |
SCHWIENTEK M, EINSIEDL F, STICHLER W, et al. Evidence for denitrification regulated by pyrite oxidation in a heterogeneous porous groundwater system[J]. Chemical Geology, 2008, 255(1): 60-67. |
| [20] |
HAYAKAWA A, HATAKEYAMA M, ASANO R, et al. 2013. Nitrate reduction coupled with pyrite oxidation in the surface sediments of a sulfide-Rich ecosystem[J]. Journal of Geophysical Rsearch:Biogeosciences, 2013, 118(2): 639-649. DOI:10.1002/jgrg.20060 |
| [21] |
HAAIJER S C M, LAMERS L P M, SMOLDERS A J P, et al. Iron sulfide and pyrite as potential electron donors for microbial nitrate reduction in freshwater wetlands[J]. Geomicrobiology Journal, 2007, 24(5): 391-401. DOI:10.1080/01490450701436489 |
| [22] |
SCHIPPERS A, JØRGENSEN B B. Biogeochemistry of pyrite and iron sulfide oxidation in marine sediments[J]. Geochimica et Cosmochimica Acta, 2002, 66(1): 85-92. DOI:10.1016/S0016-7037(01)00745-1 |
| [23] |
FDZ-POLANCO F, FDZ-POLANCO M, FERNANDEZ N, et al. New processes for simultaneous removal of nitrogen and sulfur under anearobic conditions[J]. Water Research, 2001, 35(4): 1111-1114. DOI:10.1016/S0043-1354(00)00474-7 |
| [24] |
董凌霄. 硫酸盐还原对氨氧化的影响及其抑制特性研究[J]. 西安建筑科技大学, 2006, 38(3): 425-429. DOI:10.3969/j.issn.1006-7930.2006.03.024 |
| [25] |
SHEN J P, XU Z H, HE J Z. Frontiers in the microbial processes of ammonia oxidation in soils and sediments[J]. Journal of Soils Sediments, 2014, 14(6): 1023-1029. DOI:10.1007/s11368-014-0872-x |
| [26] |
DUMONT M G, MURRELL J C. Stable isotope probing-linking microbial identity to function[J]. Nature Reviews Microbiology, 2005, 3(6): 499-504. DOI:10.1038/nrmicro1162 |
| [27] |
BRUNET R C, GARCIA-GIL L J. Sulfide-induced dissimilatory nitrate reduction to ammonia in anaerobic freshwater sediments[J]. FEMS Microbiology Ecology, 1996, 21(2): 131-138. DOI:10.1111/fem.1996.21.issue-2 |
| [28] |
LU W W, ZHANG H L, SHI W M. Dissimilatory nitrate reduction to ammonium in an anaerobic agricultural soil as affected by glucose and free sulfide[J]. European Journal of Soil Biology, 2013, 58: 98-104. DOI:10.1016/j.ejsobi.2013.07.003 |




