2. 华东师范大学 生态与环境科学学院, 上海 200062
2. School of Ecological and Environmental Sciences, East China Normal University, Shanghai 200062, China
硅藻是一类能进行光合作用的自养单细胞藻类, 全球目前已知大约有10 000~ 12 000种, 是水生生态系统中重要的初级生产者, 贡献约四分之一的全球初级生产力, 对驱动硅和碳的生物地球化学循环有着重要作用[1].硅藻生命周期短、繁殖速度快、种类多、分布广[2-4], 同时, 硅藻对水体中生化指标反应灵敏, 是海洋环境变化常用的指示生物之一[5-7].硅藻的典型特征是有一层由硅质构成的硬壳细胞壁, 该细胞壁是通过生物矿化过程吸收硅酸盐所形成的[8-10], 在保护硅藻细胞免受其他浮游生物捕食的同时, 壳体上微孔的特殊结构还可以充分帮助硅藻有效获取二氧化碳进行光合作用[11], 所以硅元素对于硅藻的生长发育必不可少[12-13].虽然地球上硅元素含量丰富, 但海洋生态系统中溶解硅的含量却较少[14].因此, 硅元素是限制海洋初级生产力的重要因子, 影响着藻类群落的演替[15].
舟形藻(Navicula arenaria var. rostellata)隶属于硅藻门羽纹硅藻纲, 是一种分布广泛的单细胞藻类, 不仅含有丰富的饱和及不饱和脂肪酸和蛋白质, 而且在水污染处理有着非常重要的作用[16].舟形藻也是热带河流的富营养化指示种和大量水生生物的主要食物来源(食物链中的关键种)[17].与其他羽纹纲藻类一样, 舟形藻细胞壁上有一个狭长的壳缝, 其通过壳缝向外分泌胞外聚合物(extracellular polymeric substance, 以下简称EPS), 硅藻分泌的EPS使自身发生向前或向后的运动[18].硅藻的运动具有重要的生物学意义, 可以让硅藻迁徙到更容易获得光照和营养物充足的区域且可以让处在异地的同一物种之间有机会进行有性繁殖, 从而优化基因[19-20]. EPS不仅可以作为保护层阻止外界有毒物质的入侵, 还可以在细胞表面固定基质聚合其他细胞形成生物膜, 这种生物膜对提高底栖硅藻生活所需的淤泥滩的稳定性具有重要作用, 也为资源极度贫瘠下的饥饿细胞提供了能量与碳源, 有利于微生物和硅藻附着并生长繁殖[21].但EPS过多分泌形成的生物膜会导致海洋生物污损(marine biofouling)现象和海雪(marine snow)爆发, 给全球渔业和航运业带来严重灾害[22-23].生物膜的形成有助于硅藻的大量繁殖, 易产生硅藻水华现象.硅藻水华产生的藻毒素和腥臭味不仅会破环景观环境, 而且会导致水生生物大量死亡, 对水产行业造成巨大损失[24-25].
硅藻水华现象、海洋生物污损现象及海雪爆发是当前的研究热门问题之一, 国内研究多集中在环境因子(如光照、温度)和营养条件(如氮、磷、硅和铁)对硅藻生长速率以及EPS分泌的影响[26-29], 而关于硅藻的一些个体运动行为却鲜有研究.近年来, 国外有研究表明, 硅藻中的菱形藻在有局部溶解硅源的情况下, 会做趋向硅源的运动[30].硅在均质环境中并非直线运动而是一种恒速画弧运动, 这种画弧运动相比直线运动扩散速率更慢, 虽不易大规模地搜寻食物, 但局部特定区域的多次重复滑行对生物膜的有效建立具有重要作用[31].然而, 国内外对于不同硅酸盐浓度对硅藻运动行为影响的研究目前较为匮乏.
本研究利用先进的显微技术, 追踪不同硅酸盐浓度下的舟形藻个体运动行为, 并对不同硅酸盐浓度环境下藻类个体的扩散速率、运动速度和圆弧半径等进行分析, 硅酸盐浓度依赖下的舟形藻个体运动行为的研究有利于加深对于硅藻觅食策略和聚集行为的理解, 以期为探讨生物膜的快速形成, 为海洋生物污损和海雪的触发提供参考意见.此外, 从个体细胞角度对硅藻运动行为的定量研究, 可以更加准确地评估硅藻在液体中扩散速率, 对有效控制春季硅藻水华的管理和爆发机制提供新的认识.
1 材料与方法 1.1 实验材料及培养条件分析所用舟形藻藻种由比利时根特大学WimVyverman教授课题组惠赠, 目前于上海市华东师范大学河口海岸学国家重点实验室保存.舟形藻所用培养基为标准的f/2+Si培养基, 其中硅酸盐浓度为30 mg/L.将舟形藻置于20 ℃, 100 r/min的光照培养箱中摇晃培养, 光照强度为2 000 lx以及光暗周期为12 h/12 h(白天/黑夜).舟形藻藻种培养至对数生长期时进行实验.
1.2 样品的准备取培养15 d处于对数期的500 μL舟形藻上清液, 将舟形藻藻液离心(6 000 r/min, 2 min).移除上清液后加入新配好的不同硅酸盐浓度但其他营养盐浓度相同的新培养基(硅酸盐浓度分别为1、15、30、60、120和240 mg/L), 轻缓混匀使得舟形藻适应新的营养环境.海洋中硅限制藻类生长的临界浓度约为1 mg/L左右, 因此小于此浓度的定义为微量硅酸盐浓度, 即本研究中的1 mg/L Na2SiO3.平时采用的标准f/2+Si培养基中硅酸盐浓度为30 mg/L, 本实验定义0.5倍标准培养基配方硅酸盐浓度为低硅酸盐浓度(15 mg/L, Na2SiO3); 定义1~ 2倍标准培养基配方硅酸盐浓度为中硅酸盐浓度(30 mg/L, Na2SiO3; 60 mg/L, Na2SiO3); 定义4~ 8倍标准培养基配方硅酸盐浓度为高硅酸盐浓度(120 mg/L, Na2SiO3; 240 mg/L, Na2SiO3).
1.3 数据的采集为了防止水分蒸发并获得长时间数据, 取70 μL舟形藻藻液加入到专用硅胶片制作的腔室中并盖上盖玻片, 固定空间的腔室可以提供静态水动力环境.在尼康Ti-E显微镜6倍物镜下明场观察.待装置制作好后, 等待30 min, 待液面稳定, 样品中藻个体沉降到载玻片表面且活性达到70%以上时开始录制, 图像采集使用PCO-sCMOS高速相机, NIS-Elements软件同步运行.视频为ND格式, 1秒1帧, 每次实验至少拍摄1 h, 像素为2 560× 2 156 pixels, 转化率1.08 μm/pixel, 观测视野范围实际为2 764 μm× 2 328 μm, 可满足实验采集图像并分析的需求.实验结束后, 将视频导出使用MATLAB软件进行图像处理及分析. MATLAB程序包括背景减噪、藻类识别追踪、轨迹平滑以及后期的数据输出, 从而快速方便准确地获得藻类运动中的个体信息.
1.4 舟形藻个体识别利用MATLAB程序读入视频后, 第一步利用imtophat函数进行顶帽变换, 补偿不均匀的背景亮度, 最终得到背景均衡的图像.第二步利用imfilter函数中的高斯滤波使得图片更平滑.第三步利用im2bw函数, 将图像转化为二值化图像并显示, 利用添加的一个MATLAB框选程序, 选择一个典型舟形藻, 设定阈值, 默认小于和大于阈值的为噪点或细菌, 程序自动追踪满足条件的舟形藻.第四步, 利用imfill函数, 将舟形藻图像中空洞补全.经过以上四步处理, 就可以准确获得藻类的二值图像.
1.5 舟形藻轨迹追踪利用regionprops函数来获取藻类的轨迹信息, regionprops函数是用来度量图像区域面积属性的函数.舟形藻为椭圆形, 该函数用椭圆拟合可以获得每个舟形藻区域具有相同标准二阶中心矩的椭圆的质心、离心率以及长轴与X轴的夹角.获得数据为每一帧时刻每一个藻类的位置信息.得到位置信息为像素点信息, 实际坐标位置需要乘以转化率得到实际坐标信息.利用相邻两帧舟形藻的位置信息, 将位置关系对应的舟形藻连接得到运动轨迹, 并对轨迹进行平滑处理, 得到最终藻类位置信息.
1.6 藻类数据的筛选及计算因为死细胞的存在或者细胞碰撞会降低数据分析的准确性.为了准确分析藻类细胞个体的轨迹, 定义平均运动速度小于2 μm/s的细胞个体为死亡细胞.并对碰撞的藻类细胞的轨迹线进行人工识别, 手动连接, 保证数据的准确性.此外, 实际分析视频时间为1 h, 数据中追踪时间过低(视野内游走时间小于5 min)的藻类运动轨迹被舍弃.对轨迹坐标进行计算, 可以得到每一步的夹角, 利用连续坐标位置差分可以得到每一帧的步长以及每一秒的速度.
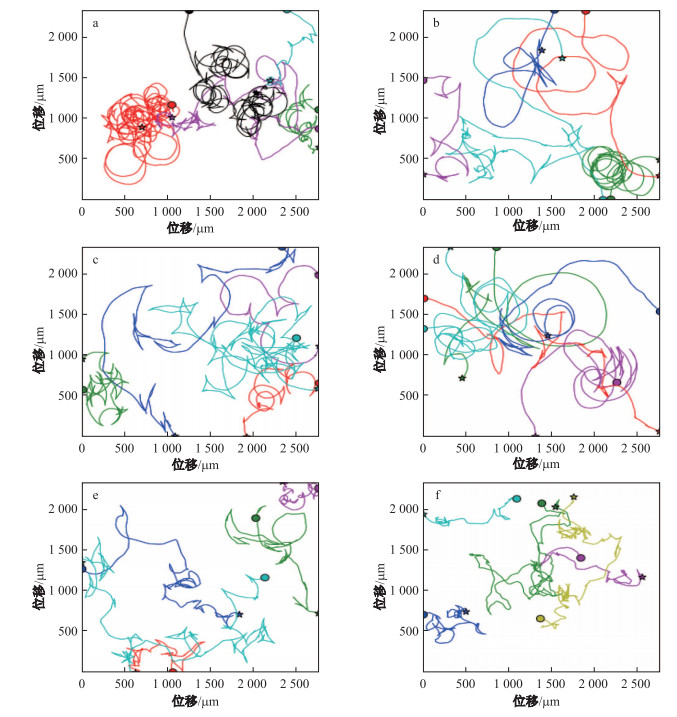
2 结 果 2.1 不同硅酸盐浓度下舟形藻的运动轨迹图 1为不同硅酸盐浓度下舟形藻细胞个体的运动轨迹, 其中硅酸盐浓度分别为图 1(a) 1 mg/L、图 1(b) 15 mg/L、图 1(c) 30 mg/L、图 1(d) 60 mg/L、图 1(e) 120 mg/L和图 1(f) 240 mg/L.由图 1可以发现不同硅酸盐浓度下舟形藻的运动轨迹略有不同, 运动轨迹定性地反映了其依赖于硅酸盐浓度的动力学特征.总体来说, 不同硅酸盐浓度下舟形藻的运动轨迹都存在大量圆弧并伴随少量倒退的行为, 并非简单的直线弹道运动, 与羽纹硅藻纲的菱形藻的运动行为相似[31].具体来说, 如图 1(a)所示, 在微量硅酸钠浓度(1 mg/L, Na2SiO3)下, 运动圆弧半径相对较小; 如图 1(b——d)所示, 在低硅酸盐浓度(15 mg/L, Na2SiO3)和中硅酸盐浓度(30 mg/L, Na2SiO3; 60 mg/L, Na2SiO3)下, 运动圆弧半径相对较大; 如图 1(e——f)所示, 在高硅酸盐浓度(120 mg/L, Na2SiO3; 240 mg/L, Na2SiO3)下, 舟形藻局部倒退行为较多.
|
注:五角星表示每条轨迹起点, 圆形表示每条轨迹终点, 每一条轨迹至少在视野内运动5 min以上 图 1 不同硅酸盐浓度下舟形藻典型运动轨迹 |
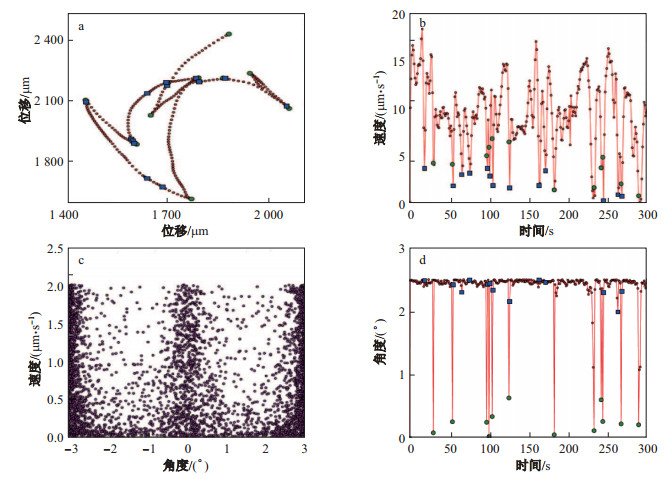
图 2(a)为一条硅酸盐浓度为30 mg/L的典型舟形藻运动轨迹图, 时长为300 s, 并绘制出轨迹速度与角度随时间变化的图 2(b)与图 2(d).可以发现在倒退时刻前后(夹角小于90°时定义为倒退点, 用绿色圆点表示)及圆弧运动停顿时刻(用蓝色方块表示)运动速度显著降低.此结论与图 2(c)结论符合, 即低速时刻(瞬时速度小于2 μ m/s)更多出现在画弧(接近180°和倒退(接近0°)前后.而通过观察所有浓度下145条舟形藻运动轨迹发现, 其运动方式主要包括三步骤: ①长时间的非恒速画弧(顺时针或逆时针)运动, 曲率基本不变; ②瞬时的倒退行为, 此时运动方向发生变化; ③再一次的长时间的非恒速画弧(顺时针或逆时针)运动, 曲率基本不变.
|
图 2 (a) 30 mg/L硅酸盐浓度下一条典型轨迹舟形藻运动300 s的轨迹图; (b)舟形藻的运动速度随时间变化图; (c)舟形藻低速时刻角度速度分布图; (d)舟形藻的角度随时间变化图 Fig.2 (a) A representative trajectory of Navicula arenaria var. rostellata under Na2SiO3 30 mg/L over 5 minutes; (b) Velocity distribution and angle distribution at low speed; (c) Speed variation diagram |
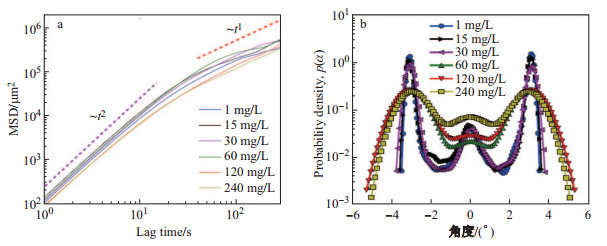
运动行为研究中, 采用均方差位移来对细胞的运动轨迹进行评价, 即
|
图 3 不同硅酸盐浓度下舟形藻的均方差位移(a)及夹角分布(b) Fig.3 Navicula arenaria var. rostellata distribution of the MSD (a) and motion angle (b) under different concentrations of Na2SiO3 |
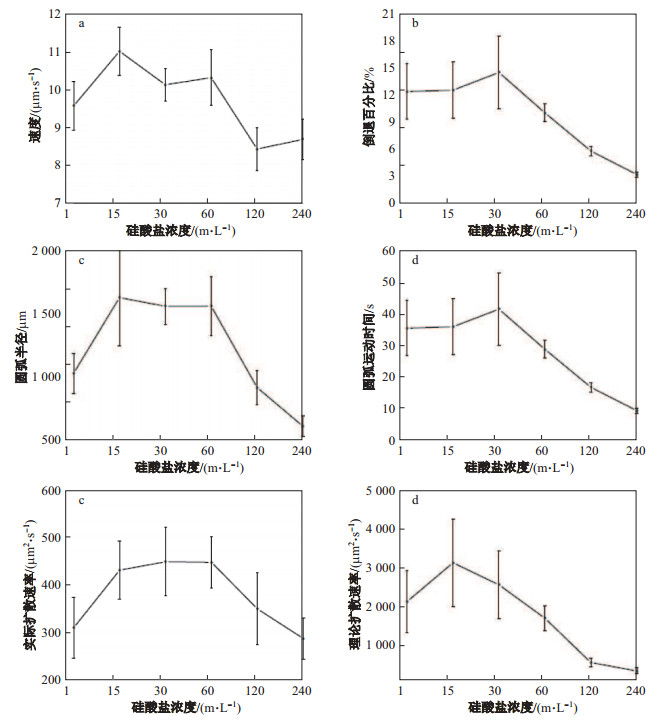
图 4(a)为不同硅酸盐浓度下舟形藻的速度变化图, 可以发现微量硅酸盐(1 mg/L, Na2SiO3)和高硅酸盐浓度(120 mg/L, Na2SiO3; 240 mg/L, Na2SiO3)下运动速度较慢, 中硅酸盐浓度(30 mg/L, Na2SiO3; 60 mg/L, Na2SiO3)下运动速度较快, 低硅酸盐浓度(15 mg/L, Na2SiO3)下运动速度最快.图 4(b)为不同硅酸盐浓度下舟形藻的倒退点占比的变化图, 明显可见高硅酸盐浓度(120 mg/L, Na2SiO3; 240 mg/L, Na2SiO3)下倒退点百分比更多: 240 mg/L硅酸盐浓度下倒退点占比为16.93{%}, 120 mg/L硅酸盐浓度下倒退点占比为7.44{%}, 倒退点的频繁出现可能会导致更多小步长和低速轨迹的产生.此外其中低硅酸盐浓度(15 mg/L, Na2SiO3)下倒退点占比为5.08{%}, 相比微量硅酸盐(1 mg/L, Na2SiO3)和中硅酸盐浓度(30 mg/L, Na2SiO3; 60 mg/L, Na2SiO3)下多0.5%左右, 具体分析详见讨论3.2节.图 4(c)为不同硅酸盐浓度下舟形藻运动的圆弧运动半径变化图, 由3个连续轨迹点可以确定一个圆, 可得圆的半径及曲率, 因倒退点半径极小故先去除倒退点时刻的半径后绘制出图 4(c).由图 4(c)可以发现在微量硅酸盐浓度(1 mg/L, Na2SiO3)和高硅酸盐浓度(120 mg/L, Na2SiO3; 240 mg/L, Na2SiO3)下圆弧半径明显较小, 中硅酸盐浓度(30 mg/L, Na2SiO3; 60 mg/L, Na2SiO3)下圆弧半径较大, 低硅酸盐浓度(15 mg/L, Na2SiO3)下圆弧半径最大.图 4(d)为不同硅酸盐浓度下舟形藻运动的圆弧运动时间图, 计算方式为两个倒退点之间的时间间隔, 由图 4(d)可以发现在高硅酸盐浓度(120 mg/L, Na2SiO3; 240 mg/L, Na2SiO3)下圆弧运动时间明显较小, 圆弧运动时间明显较大, 与由图 4(b)倒退点多导致圆弧运动时间较短结论吻合.图 4(e)为不同硅酸盐浓度下舟形藻的实际扩散速率变化图, 可以发现低硅酸盐浓度(15 mg/L, Na2SiO3)和中硅酸盐浓度(30 mg/L, Na2SiO3; 60 mg/L, Na2SiO3)下扩散速率较快, 微量硅酸盐浓度(1 mg/L, Na2SiO3)和高硅酸盐浓度(120 mg/L, Na2SiO3; 240 mg/L, Na2SiO3)下扩散速率较慢, 说明低硅酸盐浓度(1 mg/L, Na2SiO3)和中硅酸盐浓度(30 mg/L, Na2SiO3; 60 mg/L, Na2SiO3)相比微量硅酸盐浓度(1 mg/L, Na2SiO3)与高硅酸盐浓度(120 mg/L, Na2SiO3; 240 mg/L, Na2SiO3)单位时间内搜寻的面积相对较多, 具体分析详见讨论3.3节.图 4(f)为不同硅酸盐浓度下舟形藻的理论扩散速率变化图, 理论扩散速率假设细胞为直线运动, 计算公式为D=V2t/(1-α), 其中 V表示运动速度, t表示持续圆弧运动时间间隔, α表示倒退点间夹角余弦值的平均.以30 mg/L硅酸盐浓度为例, 根据t大于250 s小于300 s后的长尾均方差位移数据计算出实际扩散速率为425 μm2/s.根据数据(速度为10.05 μ m/s, 间隔时间为40.93 s, 角度平均余弦值为-1), 计算出理论扩散速率为2 566.48 μ m2/s, 理论扩散速率远大于实际扩散速率, 说明藻类圆弧运动相比直线运动在相同时间内从起始点出发经过的新区域的面积更少, 但在某个特定区域的重复运动较多, 分泌的EPS较多, 说明藻类圆弧运动的一种重要生物学功能是可以促进藻类生物膜的快速形成.由表 1可以看到, 不同硅浓度下微量硅酸盐浓度(1 mg/L, Na2SiO3)下和低硅酸盐浓度(15 mg/L, Na2SiO3)下实际扩散速率和理论扩散速率较大, 说明微量硅酸盐浓度(1 mg/L, Na2SiO3)和低硅酸盐浓度(15 mg/L, Na2SiO3)下圆弧运动的特定重复区域较小, 该区域可能会快速形成生物膜.高硅酸盐浓度(120 mg/L, Na2SiO3; 240 mg/L, Na2SiO3)下实际扩散速率与理论扩散速率相差不大, 说明高硅酸盐浓度(120 mg/L, Na2SiO3; 240 mg/L, Na2SiO3)下直线运动较多, 与倒退点较多吻合.而高硅酸盐浓度(120 mg/L, Na2SiO3; 240 mg/L, Na2SiO3)下圆弧半径较小, 速度较小, 说明舟形藻偏爱局部小范围运动, 也有助于生物膜的快速形成.
| 表 1 不同硅酸盐浓度下舟形藻运动信息 Tab.1 Motion information of Navicula arenaria var. Rostellata under different concentration of Na2SiO3 |
|
图 4 不同硅酸盐浓度下舟形藻的速度(a)、倒退百分比(b)、圆弧半径(c)、圆弧运动时间(d)、实际扩散速率(e)、理论扩散速率(f)的平均值 Fig.4 Navicula arenaria var. rostellata average value of the speed (a), reversal point percentage (b), circular radius (c), circular time (d), experiment diffusion coefficient (e), and theoretical diffusion coefficient (f) under different concentrations of Na2SiO3 |
微生物的运动中研究较多的是大肠杆菌, 多鞭毛的大肠杆菌的运动方式为前进——翻转, 而单鞭毛细菌溶藻弧菌运动方式为前进——倒退——轻击, 当单鞭毛顺时针时, 细菌向前运动, 当单鞭毛逆时针, 细菌向后倒退, 后退过程中, 鞭毛马达发生一种轻击, 改变运动方向, 经分析发现溶藻弧菌的轻击行为使他们更容易接近营养源[32-33].
海洋浮游生物中, 还有跳跃——下沉型和螺旋型等不同运动行为[34-35].国外研究表明, 羽纹纲的菱形藻在均质营养盐环境下为恒速圆弧运动伴随倒退行为[31], 在含有营养源环境下具有趋向营养源的宏观趋向性[30].通过实验观察, 舟形藻的个体运动行为是一种圆弧——倒退——圆弧的运动行为, 即一种大量非恒速圆弧运动(顺时针或逆时针)伴随少量的倒退行为.圆弧运动过程曲率基本维持不变, 但会有偶尔的停顿, 停顿时刻速度降低.倒退时刻运动方向发生显著变化, 此时夹角小于90°, 倒退前后运动速度降低.此外, 本研究发现硅酸盐浓度可以调控舟形藻的运动行为, 低硅酸盐浓度(15 mg/L, Na2SiO3)及中硅酸盐浓度(30 mg/L, Na2SiO3; 60 mg/L, Na2SiO3)下圆弧半径、运动速度和扩散系数较大, 微量硅酸盐浓度(1 mg/L, Na2SiO3)和高硅酸盐浓度(120 mg/L, Na2SiO3; 240 mg/L, Na2SiO3)下圆弧半径、运动速度和扩散系数较小, 高硅酸盐浓度(120 mg/L, Na2SiO3; 240 mg/L, Na2SiO3)下倒退行为较多.
3.2 硅酸盐浓度可以调控舟形藻运动行为近年来, 自推进粒子的个体属性和集体属性在各个领域被广泛研究, 最著名的是自推进Janus球状粒子和Daisuke Takagi制造的杆状人造粒子, 这类人造粒子半边镀铂半边镀金, 被置于过氧化氢水溶液中发生反应推动粒子运动.推动产生的运动行为, 如运动的方向, 不同过氧化氢浓度下粒子的运动行为等方面已经被广泛地研究[36-37].但是微观级别的生物粒子的研究却还甚少, 相比人造粒子, 生物个体差异较大, 觅食生化反应复杂, 所以微米级别的生物粒子在不同营养浓度下的个体行为的研究较少.
研究发现不同硅酸盐浓度下舟形藻整体的运动行为是短时间尺度的弹道行为, 中时间尺度超级扩散及长时间尺度的正常扩散, 此外舟形藻的运动行为受硅酸盐浓度调控, 由图 4可得如下关系. ①运动速度:低硅酸盐(15 mg/L, Na2SiO3)>中硅酸盐(30 mg/L, Na2SiO3; 60 mg/L, Na2SiO3)>微量硅酸盐(1 mg/L, Na2SiO3)>高硅酸盐(120 mg/L, Na2SiO3; 240 mg/L, Na2SiO3); ②倒退点百分比:高硅酸盐(120 mg/L, Na2SiO3; 240 mg/L, Na2SiO3) >低硅酸盐(15 mg/L, Na2SiO3)>中硅酸盐(30 mg/L, Na2SiO3; 60 mg/L, Na2SiO3)=微量硅酸盐(1 mg/L, Na2SiO3); ③圆弧半径:低硅酸盐(15 mg/L, Na2SiO3)>中硅酸盐(30 mg/L, Na2SiO3; 60 mg/L, Na2SiO3)>微量硅酸盐(1 mg/L, Na2SiO3)>高硅酸盐(120 mg/L, Na2SiO3; 240 mg/L, Na2SiO3); ④圆弧半径持续时间:中硅酸盐(30 mg/L, Na2SiO3; 60 mg/L, Na2SiO3) >低硅酸盐(15 mg/L, Na2SiO3)>微量硅酸盐(1 mg/L, Na2SiO3)>高硅酸盐(120 mg/L, Na2SiO3; 240 mg/L, Na2SiO3); ⑤扩散速率:低硅酸盐(15 mg/L, Na2SiO3)=中硅酸盐(30 mg/L, Na2SiO3; 60 mg/L, Na2SiO3)>微量硅酸盐(1 mg/L, Na2SiO3)=高硅酸盐(120 mg/L, Na2SiO3; 240 mg/L, Na2SiO3).硅元素有助于促进细胞的生长, 同时参与了藻类的生长分裂, 生物合成蛋白质和DNA的过程.微量硅酸盐浓度下(1 mg/L, Na2SiO3)藻类处于环境胁迫下, 硅元素受限导致舟形藻生长发育缓慢, 舟形藻采用大量运动速度较小, 圆弧半径较小的圆弧运动行为和少量的倒退行为, 这可能是舟形藻在低硅环境下主动适应性改变, 也可能是胁迫下的被动生理反映, 这种运动方式有助于局部快速建立生物膜, 为饥饿细胞提供适宜的栖息地, 提供营养及碳源有助于繁殖生存.在低硅酸盐浓度(1 mg/L, Na2SiO3)与中硅酸盐浓度(30 mg/L, Na2SiO3; 60 mg/L, Na2SiO3)下, 藻类圆弧运动半径及速度较大, 倒退点较少, 局部区域的重复运动较少, 长距离扩散相对较多.有研究表明, 当硅酸盐浓度在50~ 200 mg/L范围内时, 对舟形藻的生长速率有明显的促进作用[27], 此时, 环境营养适宜, 舟形藻更偏爱大范围觅食.高硅酸盐浓度(120 mg/L, Na2SiO3; 240 mg/L, Na2SiO3)下营养成分丰富, 硅藻不需要大范围搜寻食物更偏爱小范围运动, 存在大量局部倒退行为, 倒退行为较多可以表现整体运动速度较低, 圆弧半径持续时间较小以及圆弧半径较小, 此时小范围局部运动也有助于生物膜的快速建立.
3.3 硅酸盐浓度可能改变舟形藻觅食策略和聚集行为目前的随机运动方式主要有布朗运动和Lévy运动两种. 1905年爱因斯坦发表了关于布朗运动的文章, 描述这种微量规则的随机移动及其特性.而Lévy运动最早是由法国数学家分形之父伯努瓦·罗德勃罗(Benoit Mandelbrot)发现并以自已导师的名字命名, Lévy运动的典型特征是步长分布为厚尾分布, 包含大量的小步长运动和少量的大步长运动, 最初的生物学证据是1996年Viswannatha等从信天翁捕鱼的实验数据中, 发现信天翁捕鱼的轨迹正是Lévy运动[38], 很多生物学家又陆续观察到蜜蜂、麋鹿、鲨鱼和海龟等都是以Lévy运动来觅食的, 目前, T细胞、大肠杆菌、贻贝、蜜蜂甚至人类群体聚集行为, 都被论证为一种Lévy运动, Lévy运动被认为是物种为了优化觅食策略做出的自然选择[39].这种形式的运动是在整体环境中资源相对不足时采用的一种运动方式(如海洋中硅酸盐浓度不足时), 包括大量短距离的探索性运动, 也有偶尔的较长距离行走.大量的短距离运动可以保证在觅食过程中能够对周围小范围内的资源进行仔细搜寻, 而偶尔较长距离的行走又可以保证自身能够进入另一个区域, 在更广阔的范围进行搜索.
由数据可以看出, 舟形藻在低硅酸盐浓度(1 mg/L, Na2SiO3)下与中硅酸盐浓度(30 mg/L, Na2SiO3; 60 mg/L, Na2SiO3)下的实际扩散速率接近, 但运动速度更快, 圆弧半径更大, 说明行走范围更大, 而倒退点较多; 局部的小步长较多, 短距离运动较多, 所以低硅酸盐浓度(1 mg/L, Na2SiO3)下舟形藻的运动方式可能是一种Lévy运动.通过这种觅食策略, 舟形藻在资源贫瘠的环境下感知以及遍历搜寻的区域更多, 更容易遇到食物与配偶.而在高硅酸盐浓度(120 mg/L, Na2SiO3; 240 mg/L, Na2SiO3)下, 营养充分时, 舟形藻的均方差位移指数α在长时间尺度下等于1, 是一种布朗运动.此时实际扩散速率及运动速度最慢, 圆弧半径最小, 单位时间内遍历以及感知搜寻的区域较少.
在环境条件营养元素极度丰富时(用于细胞生长的硅酸盐浓度超出正常浓度4~ 8倍), 有研究表明, 当硅酸盐浓度大于200 mg/L时候, 舟形藻的生长速率显著降低, 胞外聚合物产量增加[26].此时舟形藻不必大范围搜寻食物, 只需在原地或者附近小范围运动.其所吸收的碳在用于生长所必需后, 过剩的有相当一部分以EPS的形式分泌出来, 积累过多的EPS有助于生物膜的快速有效建立, 有助于为饥饿的细胞提供碳源和营养物质[40]. EPS的分泌以及生物膜的产生造成环境总体和局部粘度的增加, 导致舟形藻运动速率的减慢及扩散速率的降低, 此时舟形藻聚集在生物膜附近生长繁殖, 形成生物群落, 可以有效地抵御外界不良环境.
4 结 论本文对不同硅酸盐浓度梯度(1、15、30、60、120和240 mg/L)下的舟形藻个体生物动力学特性(扩散速率、运动速度和圆弧半径等)进行研究分析, 发现如下结果: ①舟形藻的主要运动方式为大量非恒速圆弧运动伴随着少量的随机倒退行为; ②舟形藻在短时间尺度下呈现弹道行为; 在中时间尺度下呈现超扩散行为; 在长时间尺度下呈现正常扩散行为; ③舟形藻的运动行为显著依赖硅酸盐浓度, 微量硅酸盐浓度(1 mg/L, Na2SiO3)和高硅酸盐浓度(120 mg/L, Na2SiO3; 240 mg/L, Na2SiO3)环境下会抑制舟形藻运动, 低硅酸盐浓度(15 mg/L, Na2SiO3)和中硅酸盐浓度(30 mg/L, Na2SiO3; 60 mg/L, Na2SiO3)下会增强舟形藻的扩散系数.
硅酸盐浓度对硅藻个体运动行为影响的研究有利于帮助理解硅藻的觅食策略和聚集行为, 为进一步理解硅藻水华的发生、海洋生物污损现象和海雪现象的爆发提供思路.此外, 从个体细胞角度对硅藻运动行为的定量研究, 可以更加准确地评估硅藻在液体中的扩散速率, 对有效控制春季硅藻水华的管理和爆发机制提供新的认识.
| [1] |
SUMPER M, BRUNNER E. Learning from diatoms:Nature's tools for the production of nanostructured silica[J]. Advanced Functional Materials, 2010, 16(1): 17-26. |
| [2] |
FIELD C B, BEHRENFELD M J, RANDERSON J T, et al. Primary production of the biosphere:Integrating terrestrial and oceanic components[J]. Science, 1998, 281(5374): 237. DOI:10.1126/science.281.5374.237 |
| [3] |
SMETACEK V. Diatoms and the ocean carbon cycle[J]. Protist, 1999, 150(1): 25-32. DOI:10.1016/S1434-4610(99)70006-4 |
| [4] |
YEBRA D M, KⅡL S, DAM-JOHANSEN K. Antifouling technology-past, present and future steps towards efficient and environmentally friendly antifouling coatings[J]. Progress in Organic Coatings, 2004, 50(2): 75-104. DOI:10.1016/j.porgcoat.2003.06.001 |
| [5] |
GAISER E E. The diatoms:Applications for the environmental and earth sciences[J]. Journal of Soils & Sediments, 2011, 30(7/8): 103-104. |
| [6] |
JIANG H, ZHENG Y, RAN L, et al. Diatoms from the surface sediments of the South China Sea and their relationships to modern hydrography[J]. Marine Micropaleontology, 2004, 53(3/4): 279-292. |
| [7] |
JIANG H, BJÖRCK S, RAN L, et al. Impact of the Kuroshio Current on the South China Sea based on a 115?000 year diatom record[J]. Journal of Quaternary Science, 2010, 21(4): 377-385. |
| [8] |
NASSIF N, LIVAGE J. From diatoms to silica-based biohybrids[J]. Chemical Society Reviews, 2011, 40(2): 849-59. DOI:10.1039/C0CS00122H |
| [9] |
FAN T X, CHOW S K, ZHANG D. Biomorphic mineralization:From biology to materials[J]. Progress in Materials Science, 2009, 54(5): 542-659. DOI:10.1016/j.pmatsci.2009.02.001 |
| [10] |
GRACHEV M A, ANNENKOV V V, LIKHOSHWAY Y V. Silicon nanotechnologies of pigmented heterokonts[J]. Bioessays News & Reviews in Molecular Cellular & Developmental Biology, 2008, 30(4): 328-37. |
| [11] |
FUHRMANN. Hammerzeh tut weh-diese und andere Zehendeformitäten[J]. Therapeutische Umschau, 2004, 61(7): 417-420. DOI:10.1024/0040-5930.61.7.417 |
| [12] |
SEUNG WON JUNG, OH YOUN KWON, JIN HWAN LEE, et al. Effects of water temperature and silicate on the winter blooming diatom Stephanodiscus hantzschii (Bacillariophyceae) growing in eutrophic conditions in the lower Han River, South Korea[J]. Journal of Freshwater Ecology, 2009, 24(2): 219-226. DOI:10.1080/02705060.2009.9664286 |
| [13] |
MARTIN JÉZÉQUEL V, HILDEBRAND M, BRZEZINSKI M A. Silicon metabolism in diatoms:Implications for growth[J]. Journal of Phycology, 2010, 36(5): 821-840. |
| [14] |
LEWIN J. Silicon metabolism in diatoms:5. Germanium dioxide, a specific inhibitor of diatom growth[J]. Phycologia, 1966, 6(1): 1-12. DOI:10.2216/i0031-8884-6-1-1.1 |
| [15] |
EGGE J K, AKSNES D L. Silicate as regulating nutrient in phytoplankton competition[J]. Marine Ecology Progress, 1992, 83(2/3): 281-289. |
| [16] |
杨利敏.舟形藻对造纸废水中COD去除效率及其影响因素的研究[D].武汉: 华中师范大学, 2011.
|
| [17] |
李国忱, 刘录三, 汪星, 等. 硅藻在河流健康评价中的应用研究进展[J]. 应用生态学报, 2012, 23(9): 2617-2624. |
| [18] |
MOLINO P J, WETHERBEE R. The biology of biofouling diatoms and their role in the development of microbial slimes[J]. Biofouling, 2008, 24(5): 365-379. DOI:10.1080/08927010802254583 |
| [19] |
WANG J, CAO S, DU C, et al. Underwater locomotion strategy by a benthic pennate diatom Navicula sp[J]. Protoplasma, 2013, 250(5): 1203-1212. DOI:10.1007/s00709-013-0502-2 |
| [20] |
DE BROUWER J F C, WOLFSTEIN K, STAL L J. Physical characterization and diel dynamics of different fractions of extracellular polysaccharides in an axenic culture of a benthic diatom[J]. European Journal of Phycology, 2002, 37(1): 37-44. DOI:10.1017/S0967026201003419 |
| [21] |
CALLOW J A, CALLOW M E. Trends in the development of environmentally friendly fouling-resistant marine coatings[J]. Nature Communications, 2011, 2(1): 244. DOI:10.1038/ncomms1251 |
| [22] |
陈琪.海洋底栖硅藻胞外多聚物的分泌和粘附行为的研究[D].上海: 上海海洋大学, 2016.
|
| [23] |
赵守涣.丹皮酚和四种微结构硅胶材料对小舟形藻的抑制作用研究[D].上海: 上海海洋大学, 2015.
|
| [24] |
杨强, 谢平, 徐军, 等. 河流型硅藻水华研究进展[J]. 长江流域资源与环境, 2011(s1): 159-165. |
| [25] |
郑丙辉, 曹承进, 张佳磊, 等. 三峡水库支流大宁河水华特征研究[J]. 环境科学, 2009, 30(11): 3218-3226. DOI:10.3321/j.issn:0250-3301.2009.11.016 |
| [26] |
马美荣, 李朋富, 陈丽, 等. 盐度和营养限制对盐田底栖硅藻披针舟形藻生长及胞外多糖产率的影响[J]. 海洋湖沼通报, 2009(1): 95-102. DOI:10.3969/j.issn.1003-6482.2009.01.015 |
| [27] |
郑维发, 王雪梅, 王义琴, 等. 四种营养盐对舟形藻(Navicula)BT001生长速率的影响[J]. 海洋与湖沼, 2007, 38(2): 157-162. DOI:10.3321/j.issn:0029-814X.2007.02.011 |
| [28] |
刘菲菲, 冯慕华, 尚丽霞, 等. 温度对铜绿微囊藻(Microcystis aeruginosa)和鱼腥藻(Anabaena sp.)生长及胞外有机物产生的影响[J]. 湖泊科学, 2014, 26(5): 780-788. |
| [29] |
曲青梅.舟形藻悬浮培养条件优化及营养成分分析[D].山东烟台: 鲁东大学, 2015.
|
| [30] |
BONDOC K G V, HEUSCHELE J, GILLARD J, et al. Selective silicate-directed motility in diatoms[J]. Nature Communications, 2016(7): 10540. |
| [31] |
GUTIÉRREZ-MEDINA B, GUERRA A J, MALDONADO A I, et al. Circular random motion in diatom gliding under isotropic conditions[J]. Physical Biology, 2014, 11(6): 066006. DOI:10.1088/1478-3975/11/6/066006 |
| [32] |
STOCKER R. Reverse and flick:Hybrid locomotion in bacteria[J]. Proceedings of the National Academy of Sciences of the United States of America, 2011, 108(7): 2635-2636. DOI:10.1073/pnas.1019199108 |
| [33] |
XIE L, ALTINDAL T, CHATTOPADHYAY S, et al. From the cover:Bacterial flagellum as a propeller and as a rudder for efficient chemotaxis[J]. Proceedings of the National Academy of Sciences of the United States of America, 2011, 108(6): 2246. DOI:10.1073/pnas.1011953108 |
| [34] |
JACKSON G A, KIØRBOE T. Zooplankton use of chemodetection to find and eat particles[J]. Marine Ecology Progress, 2004, 269(1): 153-162. |
| [35] |
TITELMAN J, KIØRBOE T. Predator avoidance by nauplii[J]. Marine Ecology Progress, 2003, 247(1): 137-149. |
| [36] |
HOWSE J R, JONES R A L, RYAN A J, et al. Self-motile colloidal particles:From directed propulsion to random walk[J]. Physical Review Letters, 2007, 99(4): 048102. DOI:10.1103/PhysRevLett.99.048102 |
| [37] |
TAKAGI D, BRAUNSCHWEIG A B, ZHANG J, et al. Dispersion of self-propelled rods undergoing fluctuationdriven flips[J]. Physical Review Letters, 2013, 110(3): 038301. DOI:10.1103/PhysRevLett.110.038301 |
| [38] |
VISWANATHAN G M, AFANASYEV V, BULDYREV S V, et al. Lévy flight search patterns of wandering albatrosses[J]. Nature, 1996, 381(6581): 413-415. DOI:10.1038/381413a0 |
| [39] |
VISWANATHAN G M, RAPOSO E P, LUZ M G E D. Lévy flights and superdiffusion in the context of biological encounters and random searches[J]. Physics of Life Reviews, 2008, 5(3): 133-150. DOI:10.1016/j.plrev.2008.03.002 |
| [40] |
UNDERWOOD G J C, BOULCOTT M, RAINES C A, et al. Environmental effects on exopolymer production by marine benthic diatoms:dynamics, changes in composition, and pathways of production[J]. Journal of Phycology, 2010, 40(2): 293-304. |




