苔藓植物是高等植物中最原始的一个类群, 联系着维管植物和它们的藻类祖先, 在陆生植物进化研究中发挥着关键作用; 作为自然界的拓荒者之一, 苔藓植物在防止水土流失及维持生态系统平衡方面发挥着重要的作用; 同时, 作为高等植物中物种数量仅次于被子植物的一个类群, 也是生物多样性的重要组成部分[1].但是, 由于其独特的形态、生境和生活史特点, 苔藓植物特别容易受到周围环境变化及人类活动干扰的影响.鉴于苔藓植物巨大的生态应用价值及在生物多样性中的重要地位, 其多样性保护日渐受到重视[2].对于苔藓植物来说, 其野外就地保护大多是偶然的, 主要是在保护其他物种的同时顺带实现了对其保护[1].然而, 尽管已经建立较完备的保护区网络, 位于欧洲的马卡罗尼西亚地区35种特有苔藓植物中有6种将在50年后灭绝, 即使是当地分布最广泛的种类也会达到易危甚至濒危的程度[3].因此, 开展对苔藓植物, 尤其是特有濒危种类的迁地保护尤为重要.
目前, 超低温保存技术已经在植物种质资源保存研究方面被广泛应用.国际上, 苔藓植物种质资源超低温保存研究主要集中在对其配子体及原丝体保存研究方面, 缺乏对孢子体的保存研究[4-7].这主要有两方面原因, 一是因为苔藓植物中雌雄异株比例较高, 有70%的苔类和60%的藓类为雌雄异株, 这些类群常常因为雌、雄株之间的距离较大而导致卵细胞很难受精, 从而导致孢子体材料很难获得[1];二是因为苔藓植物的孢子体非常微小, 在野外很容易被忽视.因而, 同样作为孢子植物, 有很多关于蕨类植物孢子的超低温保存的研究, 有关苔藓植物的孢子保存研究的报道却很少[8-9].然而, 苔藓植物配子体及原丝体的超低温保存效果与其植物体在自然环境中对干燥和低温的忍耐能力紧密相关, 需要在保存前进行干燥及低温预处理.而且, 一些生长在湿润环境中的种类极易受干燥处理的影响, 超低温保存后的成活率非常低, 比如采自湿润生境中的2种泥炭藓(Sphagnum girgensohnii和S. russowii), 其配子体在超低温保存后的再生率仅为20%[6, 10].相反, 不同生境中的苔藓植物孢子似乎受干燥处理影响不大[11].因此, 苔藓植物孢子的超低温保存有可能解决湿润生境种类的种质资源超低温保存问题, 而且很有可能代表一种简单、稳定又便捷的苔藓植物超低温保存手段.
我们在2014年初步探索并确定了苔藓植物孢子超低温保存方法, 并将其成功应用于细叶小羽藓(Haplocladium microphyllum)的超低温保存[12].但是, 该方法只在一个种中得到检验, 其适用性还是未知的.为了检验超低温保存方法的适用性, 本文对采自不同生境中的6种藓类孢子进行超低温保存研究, 并对其中5种藓类的孢子进行不同时间梯度的超低温保存效果研究.
1 材料与方法 1.1 实验材料6种藓类孢子体于2013
| 表 1 实验材料 Tab. 1 Materials used in experiment |
参照李秋萍等方法[12], 在体式显微镜下选择色泽相近、体型饱满的成熟孢蒴, 分别置于硅胶中0 h (CK)、5 h、10 h和20 h后取出, 投入1.5 mL的冻存管中, 然后分别于15
参照李秋萍等方法[12], 在各种藓类孢子最适的处理条件下, 选取成熟的孢蒴通过设置时间梯度(1 d、15 d、30 d、90 d和180 d)进行不同时间的保存实验.每个处理条件保存7—8个成熟的孢蒴, 保存不同时间后取出, 采用室温下自来水冲洗化冻, 然后接种至Knop固体培养基上培养.接种8 d后于显微镜下检测孢子的平均萌发率.在统计萌发率的时候, 每个处理条件接种3个培养皿, 每个培养皿选取3个视野于显微镜下观察, 统计孢子平均萌发率.由于所需孢蒴数量较多, 有部分藓类因为孢蒴采集数量不能满足时间梯度实验, 故日本曲尾藓未进行不同时间梯度保存实验, 长蒴藓、葫芦藓和丝瓜藓的时间梯度只设置到30 d.
1.4 数据分析使用Excel 2010进行数据处理, 采用SPSS19.0程序对实验结果进行统计分析, 均值的多重比较采用邓肯氏(Duncan)新复极差检验和LSD法检验[13], 检验水平
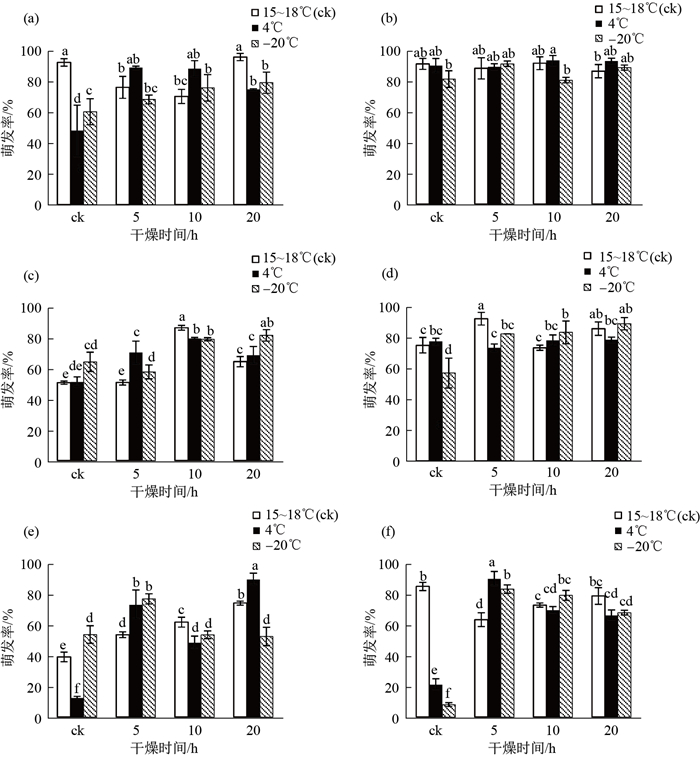
图 1显示, 干燥和低温预处理都影响到孢子的萌发率, 6种藓类孢子萌发率在最适处理条件下均大于87%.长蒴藓(T. longicollis)孢子在15
|
注: (a)长蒴藓; (b)葫芦藓; (c)卵蒴真藓; (d)丛生真藓; (e)丝瓜藓;
(f)日本曲尾藓.萌发率用平均值和标准差表示, 字母不同表示差异显著( |
不同生境中的种类所需的干燥和低温预处理条件稍有不同, 对于采自干旱生境中的长蒴藓和丛生真藓, 只需要对其孢子进行不同时间长度的硅胶干燥处理就可达到最高萌发率(分别为96.21%和92.01%).但是, 对于采自湿润生境中的日本曲尾藓和丝瓜藓, 孢子需要分别在4 ℃下干燥5 h和20 h才能达到最高萌发率(分别为91.22%和90.86%).对于常见种葫芦藓, 不同处理条件下的孢子萌发率均表现出较高水平(81.43%
在最适处理条件下, 5种藓类孢子在超低温保存1 d后均表现出最高的萌发率(87.25%
| 表 2 5种藓类孢子超低温保存不同时间后萌发率比较 Tab. 2 Comparison of germination rates for spores from five moss species under different |
由于苔藓植物配子体的结构简单以及消毒困难, 其超低温保存时需要使用无菌培养的材料, 这一过程需要耗费较长时间, 而且配子体在超低温保存过程中必须借助特定的冰冻保护剂才能避免在冷冻过程中受到伤害.即使这样, 配子体的超低温保存成功还与物种固有的对干燥和低温的耐受力有关[6, 10].而苔藓植物孢子的抗旱性能已被证明与其生境并无太大关系[11], 这可能与孢子表面具有孢粉素等化合物而赋予其较强的抗物理损伤和逆境性能有关[1].除此之外, 苔藓植物的孢子在水势低至--2 MPa时仍可以萌发, 而大多数种子在这种水势下则失去萌发能力[14].这些特点都表明了苔藓植物孢子非常适合于超低温保存, 而且可能代表一种简单、稳定、高效的苔藓植物种质资源保存材料, 这一结论在本研究中得到了证明.
相对于低温预处理, 本研究表明超低温保存前的干燥处理有助于孢子的保存.实验数据显示经过干燥处理的6种藓类孢子萌发率普遍大于未经干燥的孢子.超低温保存的成功与否所遇到的最大挑战是保存材料是否具备在极端低温下忍耐冷却和复苏的能力, 而在这个冷冻过程中的由水向冰过渡所引发的生物物理变化被认为是造成机体伤害的主要原因[15].因此, 孢子含水量的控制是其保存成功与否的关键[12].为了避免这种伤害, 有必要对超低温保存前的植物材料进行脱水处理[6].因为本文重点在于检测一种保存方法在保存不同生境中孢子的适用性, 故未对孢子的含水量进行定量测定.但是, 对于采自湿润生境中的藓类孢子比如日本曲尾藓和丝瓜藓, 干燥加低温预处理则为最佳的处理条件, 这可能表明相对较湿润的孢子在超低温保存前更需要进行低温诱导.
与李秋萍等[12]实验结果相似, 本文在对5种藓类孢子进行不同时间梯度保存效果研究时发现:孢子的平均萌发率在保存后第一天均为最高, 但随着保存时间的延长其萌发率出现先降后升又降的趋势, 而且不同保存时间内孢子萌发率表现出显著性的差异.从理论上来讲, 孢子在液氮保存情况下其物质代谢和生长活动几乎完全停止[16], 其萌发率在短期内应该不会表现出类似的显著性差异.这一异常现象在蕨类的孢子、种子植物的花粉[17], 甚至是苔藓植物芽胞中也存在[18], 推测其原因可能与保存材料在超低温保存过程中先受到伤害而又启动修复功能的过程有关[12].在接下来的研究中, 可以利用透射电镜观察不同保存时间的孢子细胞内部结构是否受到破坏, 来探讨发生这一现象可能的原因.
| [1] |
VANDERPOORTEN A, GOFFINET B. Introduction to Bryophyte[M]. Cambridge: Cambridge University Press, 2010: 1-2.
|
| [2] |
HYLANDER K, JONSSON B G. The conservation ecology of cryptogams[J]. Biological Conservation, 2007, 135(3): 311-314. DOI:10.1016/j.biocon.2006.10.019 |
| [3] |
PATIÑO J, MATEO R G, ZANATTA F, et al. Climate threat on the Macaronesian endemic bryophyte flora[J/OL]. Scientific Reports, 2016. Doi: 10.1038/srep29156. https://www.nature.com/articles/srep29156.pdf
|
| [4] |
PENCE V C. Cryopreservation of bryophytes:The effects of abscisic acid and encapsulation dehydration[J]. Bryologist, 1998, 101(2): 278-281. DOI:10.1639/0007-2745(1998)101[278:COBTEO]2.0.CO;2 |
| [5] |
BURCH J, WILKINSON T. Cryopreservation of protonemata of Ditrichum cornubicum (Paton) comparing the effectiveness of four cryoprotectant pretreatments[J]. CryoLetters, 2002, 23(3): 197-208. |
| [6] |
BURCH J. Some mosses survive cryopreservation without prior treatment[J]. Bryologist, 2003, 106(2): 270-277. DOI:10.1639/0007-2745(2003)106[0270:SMSCWP]2.0.CO;2 |
| [7] |
ROWNTREE J K, RAMSAY M M. How bryophytes came out of the cold:Successful cryopreservation of threatened species[J]. Biodiversity and Conservation, 2009, 18: 1413-1420. DOI:10.1007/s10531-008-9453-x |
| [8] |
PANGUA E, GARCIA-ALVAREZ L, PAJARÓN S. Studies on Cryptogamma crispa spore germination[J]. American Fern Journal, 1999, 89(2): 159-170. DOI:10.2307/1547350 |
| [9] |
ROGGE G D, VIANA A M, RANDI A M. Cryopreservation of spores of Dicksonia sellowiana:An endangered tree fern indigenous to south and central America[J]. CryoLetters, 2000, 21: 223-230. |
| [10] |
SEGRETO R, HASSEL K, BARDAL R, et al. Desiccation tolerance and natural cold acclimation allow cryopreservation of bryophytes without pretreatment or use of cryoprotectants[J]. Bryologist, 2010, 113(4): 760-769. DOI:10.1639/0007-2745-113.4.760 |
| [11] |
VAN ZANTEN B O, GRADSTEIN S R. Experimental dispersal geography of neotropical liverworts[J]. Beiheft zur Nova Hedwigia, 1988, 90: 41-94. |
| [12] |
李秋萍, 姜丽佳, 鲁蓓蓓, 等. 细叶小羽藓孢子的超低温保存[J]. 华东师范大学学报(自然科学版), 2014(6): 121-125. DOI:10.3969/j.issn.1000-5641.2014.06.016 |
| [13] |
杜荣骞. 生物统计学[M]. 北京: 高等教育出版社, 2003.
|
| [14] |
WIKLUND K, RYDIN H. Ecophysiological constraints on spore establishment in bryophytes[J]. Functional Ecology, 2004, 18(6): 907-913. DOI:10.1111/fec.2004.18.issue-6 |
| [15] |
FULLER B J. Cryoprotectants:the essential antifreezes to protect life in the frozen state[J]. CryoLetters, 2004, 25(6): 375-388. |
| [16] |
简令成. 低温生物学与植物种质的长期保存[J]. 植物学通报, 1998, 5(2): 65-68. |
| [17] |
徐艳, 刘燕, 石雷. 大叶黑桫椤孢子超低温保存[J]. 植物生理学通讯, 2006, 42(1): 55-57. |
| [18] |
WU S P, QIN Z Z, XIAO T Z, et al. Cryopreservation of gemmae of Marchantia polymorpha L. (Marchantiophyta, Marchantiaceae) without prior pretreatment[J]. CryoLetters, 2015, 36(2): 91-96. |




